TEKST DANIQUE VAN DIEPEN1,2, ADRIAAN ANTONIS1,2, HEATHER GRAHAM2
De stille insluiper: boviene besnoitiose
Een ‘olifantshuid’, verhoogd melkcelgetal bij koeien, onvruchtbaarheid bij stieren en kenmerkende cysten in sclera en vulva zijn enkele symptomen van een infectie met Besnoitia besnoiti. De parasiet, die oorspronkelijk voorkomt in Afrika, Azië en Zuid-Europa, breidt zich de laatste jaren uit naar Noord-Europa, met uitbraken in Duitsland en België. Verspreiding vindt voornamelijk plaats via vectoren maar ook door middel van direct contact via huidlaesies of tijdens een natuurlijke dekking. De infectie verloopt van een acuut stadiumlijkend op blauwtong naar een chronisch stadium met opvallende huidveranderingen. Behandeling of vaccinatie is niet beschikbaar.
1 Sustainable Ruminant Health (SRH) groep, afdeling Landbouwhuisdieren, departement Population Health Sciences (PHS), faculteit Diergeneeskunde, Universiteit Utrecht.
2 Wageningen Bioveterinary Research (WBVR), Wageningen University and Research (WUR), Lelystad.
In Nederland is nog geen met B. besnoiti geïnfecteerd rund aangetroffen, maar er wordt ook niet of nauwelijks op getest. Met meer dan 10.000 geïmporteerde runderen uit endemische landen per jaar, is het niet de vraag of, maar wanneer de eerste casus zich aandient. Tijd om de bekendheid te vergroten: maak kennis met boviene besnoitiose.
LEVENSCYCLUS
B. besnoiti is een cyste-vormende protozo en is verwant aan Toxoplasma gondii en Neospora caninum (1). De parasiet kent een heteroxene levenscyclus en heeft dus meerdere gastheren nodig. Recente studies tonen aan dat niet alleen runderen, maar ook reeën en edelherten als tussengastheer kunnen dienen. Gezien de lage aangetoonde prevalentie bij reeën en edelherten is het risico op overdracht naar runderen klein (2). Hoewel er geen sluitend bewijs is, wordt vermoed dat de kat, of een andere carnivoor, eindgastheer is (3-5). Recentelijk is het parasitaire DNA aangetoond in feces van een rode vos in Spanje en zelfs in Nederland in feces van een meervleermuis ( Myotis dasycneme ) (6, 7). Vermoed wordt dat deze vleermuis afkomstig is uit een endemisch gebied. De definitieve eindgastheer blijft daarmee onbekend.
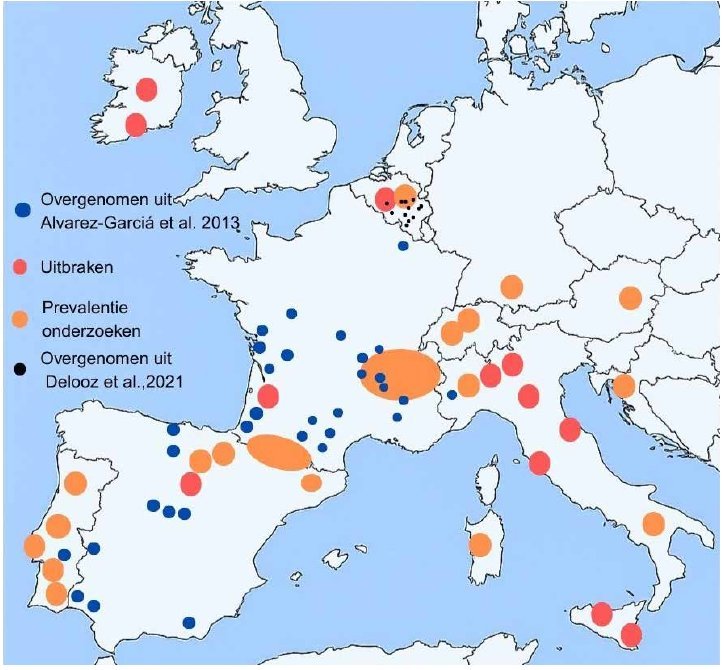
Figuur 1. Overzicht Besnoitia besnoiti in Europa. Uitbraken (rood), prevalentie studies (oranje), overgenomen casussen uit Alvarez-Garciá et al., 2013 (blauw), overgenomen casussen uit Delooz et al., 2021 (zwart).
EPIDEMIOLOGIE
Boviene besnoitiose komt endemisch voor in Spanje, Portugal, Frankrijk en Italië (8). In Zwitserland, Hongarije, Griekenland en Ierland zijn uitbraken of enkele positieve gevallen beschreven en ook in onze buurlanden België en Duitsland (9-14). In niet endemische landen ontstaat een besmetting meestal na de import van een geïnfecteerd rund (15). Het is dan ook niet verwonderlijk dat de European Food Safety Authority (EFSA) boviene besnoitiose in 2010 heeft geclassificeerd als ‘emerging disease’ (8). Een overzicht van de gerapporteerde casussen is weergegeven in figuur 1.
Er bestaan epidemiologische verschillen tussen niet endemische gebieden en endemische gebieden. In endemische regio’s wordt per jaar doorgaans 1 tot 10 procent van het koppel klinisch. In niet endemische gebieden ligt dit percentage hoger en worden doorgaans na introductie bij 15 tot 40 procent van het koppel klinische symptomen waargenomen (16, 17).
De seroprevalentie ligt vrijwel altijd hoger dan het percentage klinische runderen. Zo werd tijdens een uitbraak in Spanje met negen betrokken koppels een seroprevalentie van 90,8 procent vastgesteld, terwijl slechts 43,2 procent van de dieren klinische verschijnselen vertoonde (16). Verspreiding van besnoitiose kan redelijk vlot verlopen. Zo steeg de seroprevalentie op een Frans melkveebedrijf binnen één jaar van 30 procent naar 89,47 procent (n = 71) (18). De verspreiding van B. besnoiti tussen rundveebedrijven wordt eveneens waargenomen, ondermeer door aangrenzend grazen of de lokale verkoop van geïnfecteerde runderen. In België leidde de import van één geïnfecteerde stier bij drie andere bedrijven tot uitbraken (19).
TRANSMISSIE
De transmissie van B. besnoiti vindt horizontaal plaats. Transmissie door vectoren speelt daarbij een grote rol. Bloedzuigende insecten, zoals dazen en stalvliegen, kunnen de parasiet mechanisch overdragen (20). Deze insecten dragen B. besnoiti gedurende korte tijd bij zich; stalvliegen ongeveer één uur en dazen tot 24 uur (15, 21). Verspreiding verloopt daarom minder snel dan bij het blauwtongvirus waarbij de knutten het virus levenslang (1-2 maanden) bij zich dragen (22, 23). Daarnaast is voor een succesvolle overdracht een minimaal aantal insectenbeten nodig (21, 24). Hoewel infecties het hele jaar kunnen optreden, is er een duidelijke piek in de zomermaanden, samenhangend met de hogere activiteit van vliegen (18, 24). Regelmatig aanbrengen van pyrethroïde-insecticiden kan mogelijk bijdragen aan het verminderen van insectenbeten, maar er bestaat nog geen goed werkend protocol om stekende vliegen volledig te voorkomen (8).
Ook is overdracht mogelijk via direct contact met wonden of door natuurlijke dekking met een geïnfecteerde stier. Daarnaast kan de parasiet iatrogeen worden overgedragen bij hergebruik van naalden (8, 24, 25). Door natuurlijke dekking kunnen aanwezige cysten openbarsten en daardoor de parasiet overdragen. Er is een verhoogd overdrachtsrisico voor natuurlijke dekking vastgesteld wanneer seronegatieve koeien worden gedekt door een seropositieve stier. Het risico werd niet aangetoond voor seronegatieve stieren die een seropositieve koe dekten. Het aandeel van overdracht is echter klein en vectorinvloed kan niet volledig worden uitgesloten (7, 25). Overdracht via colostrum, sperma of via de placenta is niet aangetoond (26-28). Hoewel verschillende rassen, leeftijden en geslachten geïnfecteerd kunnen raken, komt de aandoening vaker voor bij oudere dieren vanwege de langer durende blootstelling aan de vector (16, 29, 30). Uit data blijkt dat vooral vleesvee besmet raakt, waarschijnlijk omdat deze dieren vaker extensief worden gehouden en daardoor mogelijk meer in contact komen met vectoren. Daarnaast wordt bij vleesvee vaker natuurlijke dekking toegepast dan bij melkvee (24, 30).
PATHOGENESE
Boviene besnoitiose verloopt in verschillende fases. In het acute stadium, waarin tachyzoïeten met hoge snelheid repliceren in macrofagen, fibroblasten en endotheelcellen, ontstaat koorts die op kan lopen tot 41,6 graden Celsius. Daarnaast kunnen aspecifieke symptomen optreden zoals anorexie, depressie, fotofobie, verminderde melkproductie, gezwollen lymfeknopen en algehele zwakte. Ook kan tachycardie, tachypneu en nasale en oculaire uitvloeiing ontstaan. Als gevolg van de hoge koorts kunnen drachtige koeien aborteren. Dit stadium duurt vaak zes tot tien dagen (31-33).
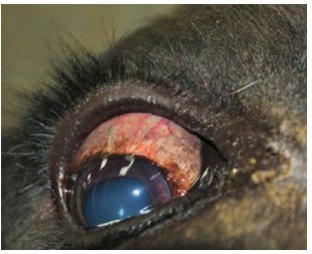
Afbeelding 2. Parasitaire cysten op de sclera.

Afbeelding 3. Het chronische stadium van besnoitiose.
Als gevolg van vasculitis, trombose en zelfs necrose van bloedvaten neemt de vaatwandpermeabiliteit af. Hierdoor ontstaat in eerste instantie oedeem rond de kop en nek, later in ventrale delen en rond gewrichten. Gewrichten worden pijnlijk en het dier kan kreupel worden. In ernstige gevallen kan er longoedeem ontstaan. Een of twee weken na de start van de acute fase neemt oedeem af (33). Het chronische stadium van de infectie wordt gekenmerkt door de vorming van cysten in de sclera, conjunctiva en vulva (zie afbeelding 2). Intern worden op diverse plekken ook cysten gevormd zoals in de bovenste luchtwegen en het distale deel van de vrouwelijke genitaal-tractus. Zelfs in het hart kunnen cysten worden aangetroffen (28). Tevens kunnen deze ontstaan in de spenen en de uier met als gevolg een verminderde elasticiteit en wondvorming (28, 33). B. besnoiti heeft een tropisme voor bindweefsel (24). De cysten, ongeveer 0,5 millimeter groot, bevatten parasieten in een slapende toestand (34). Deze ontstaan meestal zes tot zeven weken post-infectie (33). De mortaliteitsgraad is tijdens het chronische stadium doorgaans beneden de 10 procent (33). Huidveranderingen, zoals alopecia, hyperkeratose en seborroe kunnen optreden (zie afbeelding 3). Bij ernstige verstoring van de lokale circulatie kan de huid zelfs loslaten. Ook kunnen noduli verschijnen rond de oren, poten en rug. In dit stadium valt vaak ook een lage Body Condition Score op (33, 35, 36). Daarnaast kan door cysten tussen de lamellen in de klauw chronische laminitis ontstaan (36, 37). Hoewel runderen waarschijnlijk levenslang drager blijven, kunnen ze na verloop van tijd serologisch negatief testen en klinische verbetering vertonen. Serologisch komen fluctuaties voor, waardoor dieren een negatieve testuitslag kunnen hebben om later opnieuw positief te testen (38). In een Duitse studie bleek 9,4 procent van de dieren na vier jaar seronegatief en vrij van zichtbare cysten. Twee uitzonderlijke gevallen bereikten dit stadium al na 2,5 jaar (39). B. besnoiti kan het immuunsysteem van runderen moduleren, maar er is meer onderzoek nodig om te begrijpen welke effecten de parasiet op langere termijn heeft (37, 40, 41).
VRUCHTBAARHEIDSPROBLEMEN
Stieren kunnen ook vruchtbaarheidsproblemen ontwikkelen. Door laesies als gevolg van vasculitis, necrose en sclerose in de testis kan de stier permanent onvruchtbaar worden. Aantasting van de genitaaltractus leidt tot een verminderde spermascore. Of de spermakwaliteit herstelt wanneer stieren genezen, is niet bekend (28, 42-44). Bij vrouwelijke runderen kan er door de hoge koorts abortus optreden. Daarnaast worden er cysten in het distale deel van de genitaal-tractus gevonden, maar dit leidt niet tot vruchtbaarheidsproblemen (28).

VERMINDERDE MELKPRODUCTIE
De invloed van besnoitiose op de melkproductie blijkt wisselend. (45). In het acute stadium is een productiedaling waargenomen, die later herstelde (12). In een Italiaanse studie werden bij 7 van de 217 koeien in het chronische stadium significant lagere melkopbrengsten vastgesteld. Daarnaast is aangetoond dat het celgetal significant hoger ligt bij koeien met besnoitiose (gem. 300.000 cellen/ml), al werd geen directe relatie met het aantal mastitisgevallen gevonden (46).
ECONOMISCHE VERLIEZEN
Economische verliezen in de rundveehouderij ontstaan door gewichtsverlies en verminderde groei, verhoogd celgetal, abortus, vruchtbaarheidsproblemen bij stieren, en aantasting van het leer. Cijfers over de economische impact zijn in de literatuur beperkt (44). Op de Franse webpagina, La France Agricole , wordt een bedrijf beschreven, waar in 2017 de eerste klinische gevallen werden vastgesteld. Na screening van het volledige koppel bleken zeventig koeien positief. De kosten van diagnostiek en behandeling bedroegen circa 8.000 euro, naast de kosten voor afvoer en stilvallen van de verkoop. De veehouder schatte het verlies aan brutobedrijfsresultaat op ongeveer 60.000 euro (47).
DIAGNOSTIEK
Boviene besnoitiose kan diagnostisch vastgesteld worden op basis van het klinisch beeld en aanvullende diagnostiek. Cysten in de sclera, conjunctiva en vulva zijn pathognomonisch voor de aandoening. Voor aanvullende diagnostiek zijn zowel directe methoden, zoals PCR en histopathologie, als indirecte methoden, zoals serologie beschikbaar.
In de acute fase, wanneer antistoffen nog niet gevormd of aantoonbaar zijn en cysten nog ontbreken, kan de diagnose worden gesteld met een (rt-)PCR op een huidbiopt of bloedmonster (48). Recent onderzoek wijst ook op de mogelijkheid van het testen van nasale en oculaire swabs, al moet deze methode in de praktijk nog verder worden gevalideerd (49). In de chronische fase kan histopathologisch onderzoek van huid- en vaginabiopten de aanwezigheid van cysten van B. besnoiti aantonen (36). De meest toegepaste diagnostische methode is een ELISA op serum of plasma voor de detectie van antilichamen. Ook subklinisch geïnfecteerde dieren kunnen hiermee gedetecteerd worden. In Nederland wordt deze test aangeboden bij Wageningen Bioveterinary Research. Positieve resultaten moeten worden bevestigd met een Western Blot, in verband met mogelijke kruisreactiviteit met Neospora caninum en Sarcocystis spp. (33, 50).
BEHANDELINGEN
Op dit moment is er geen behandeling mogelijk. Positieve dieren dienen afgevoerd te worden (7). Experimenteel zijn er aanwijzingen voor mogelijke behandelmethoden, maar deze zijn in vivo onvoldoende onderzocht en niet beschikbaar in Europa (48, 51-56). In Zuid-Afrika en Israël wordt gevaccineerd met een levend vaccin, maar het effect is nog niet bewezen (32, 57).
PREVENTIE
Het allerbelangrijkste is te voorkomen dat de parasiet in Nederland komt. Testen vóór import is daarom cruciaal. Veehouders die runderen importeren uit landen zoals Spanje, Portugal, Frankrijk of Italië, wordt geadviseerd te testen op de aanwezigheid van antistoffen, bijvoorbeeld bij Wageningen Bioveterinary Research. Daarnaast moeten de dieren vrij zijn van pathognomonische verschijnselen en wordt aangeraden de standaard quarantainerichtlijn van vier weken aan te houden, al zullen de subklinische dragers hiermee niet worden opgemerkt (58).
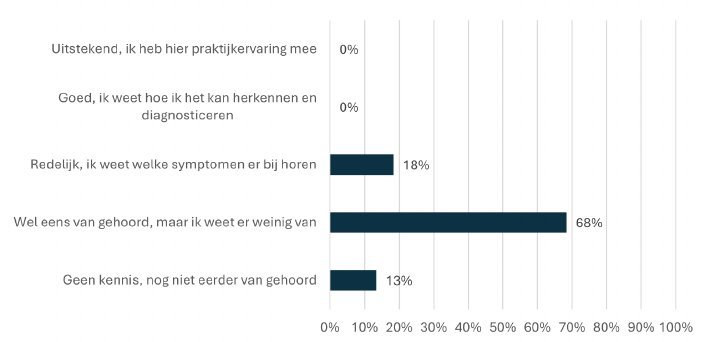
Figuur 4. Antwoorden op de enquêtevraag: “Hoe zou u uw kennisniveau over besnoitiose beoordelen?”
KENNISPEILING ONDER DIERENARTSEN
Om inzicht te krijgen in de bekendheid van besnoitiose bij rundveedierenartsen in Nederland is een vragenlijst verspreid. De respons was beperkt (n = 60) en het gaat dus niet om een representatieve steekproef. Conclusies voor gehele beroepsgroep kunnen niet worden getrokken maar de uitslagen geven wel een beeld van de huidige kennisstand. Geen van de ondervraagde dierenartsen beoordeelde zijn of haar kennisniveau als “goed”; de meesten hadden alleen gehoord over besnoitiose (zie figuur 4). In de casus van acute besnoitiose had maar 28,33 procent het opgenomen in de differentiële diagnose. In het chronische stadium werd de aandoening iets beter herkend: 40 procent plaatste het dan op de Ddx. Bij elke kennisvraag koos meer dan 20 procent voor de optie “Weet ik niet”, wat de onzekerheid onderstreept. Bovendien gaf 100 procent van de respondenten aan meer te willen weten over de aandoening.
BELANG VAN MONITORING
Voor besnoitiose geldt geen meldings- of bestrijdingsplicht en er wordt momenteel niet op gemonitord. Hierdoor bestaat het risico dat de parasiet ongemerkt Nederland binnenkomt. Goede kennis over de aandoening bij zowel de dierenarts als in de sector is van groot belang om stille verspreiding van B. besnoiti te voorkomen. Om introductie van de parasiet te voorkomen, adviseren wij bloedmonsters van runderen die worden geïmporteerd uit endemische gebieden, te laten testen op de aanwezigheid van B. besnoiti . Zo ondervangen we dat de subklinische dieren de parasiet onopgemerkt in het koppel en in Nederland kunnen verspreiden. Wageningen Bioveterinary Research biedt hiervoor een diagnostische test aan.
Met dank aan Eoin Ryan voor het gebruik van de afbeeldingen en aan Royal GD, LTO Nederland, Vee & Logistiek, CRV en LVVN voor de input. Dank ook aan alle rundveedierenartsen die deelnamen aan de enquête.
Bronnen
1. Ellis JT, Holmdahl OJ, Ryce C, Njenga JM, Harper PA, Morrison DA. Molecular phylogeny of Besnoitia and the genetic relationships among Besnoitia of cattle, wildebeest and goats. Protist. 2000;151(4):329–36.
2. Gutiérrez-Expósito D. The role of wild ruminants as reservoirs of Besnoitia besnoiti infection in cattle. Veterinary parasitology. 2016;223:7–13.
3. Diesing L. Besnoitia besnoiti: studies on the definitive host and experimental infections in cattle. Parasitology research. 1988;75(2):114–7.
4. Peteshev V, Galuzo I, Polomoshnov A. [Cats as definitive hosts of Besnoitia besnoiti]. Izvestiya Akademii Nauk Kazakskoi SSR, Seria Biologicheskaya. 1974(No.1):33–8.
5. Basso W. Exploring the life cycle of Besnoitia besnoiti – experimental infection of putative definitive and intermediate host species. Veterinary parasitology. 2011;178(3-4):223–34.
6. González-Barrio D. Molecular survey of Besnoitia spp. (Apicomplexa) in faeces from European wild mesocarnivores in Spain. Transboundary and emerging diseases. 2021;68(6):3156–66.
7. Hornok S. Screening of bat faeces for arthropod-borne apicomplexan protozoa: Babesia canis and Besnoitia besnoiti-like sequences from Chiroptera. Parasites & vectors. 2015;8:441.
8. Jacquiet P. Bovine besnoitiosis: epidemiological and clinical aspects. Veterinary parasitology. 2010;174(1-2):30–6.
9. Lesser M. First cases of besnoitiosis in cattle in Switzerland. Schweizer Archiv fur Tierheilkunde. 2012;154(11):469–74.
10. Hornok S. Bovine besnoitiosis emerging in Central-Eastern Europe, Hungary. Parasites & vectors. 2014;7:20.
11. Papadopoulos E, Arsenos G, Ptochos S, Katsoulos P, Oikonomou G, Karatzia M, et al. First report of Besnoitia besnoiti seropositive cattle in Greece. Blood. 2010.
12. Ryan EG. Bovine besnoitiosis (Besnoitia besnoiti) in an Irish dairy herd. The Veterinary record. 2016;178(24):608.
13. Rostaher A. Bovine besnoitiosis in Germany. Veterinary dermatology. 2010;21(4):329–34.
14. Vanhoudt A, Pardon B, De Schutter P, Bosseler L, Sarre C, Vercruysse J, et al. Eerste bevestigd geval van boviene besnoitiose in België bij een ingevoerde stier. Vlaams Diergeneeskundig Tijdschrift. 2015;84(4):205–11.
15. Saegerman C. First Expert Elicitation of Knowledge on Drivers of Emergence of Bovine Besnoitiosis in Europe. Pathogens (Basel, Switzerland). 2022;11(7).
16. Fernández-García A. Development and use of an indirect ELISA in an outbreak of bovine besnoitiosis in Spain. The Veterinary record. 2010;166(26):818–22.
17. Schares G. Comparative evaluation of immunofluorescent antibody and new immunoblot tests for the specific detection of antibodies against Besnoitia besnoiti tachyzoites and bradyzoites in bovine sera. Veterinary parasitology. 2010;171(1-2):32–40.
18. Liénard E. A longitudinal study of Besnoitia besnoiti infections and seasonal abundance of Stomoxys calcitrans in a dairy cattle farm of southwest France. Veterinary parasitology. 2011;177(1-2):20–7.
19. Delooz L. Emergence of Besnoitia besnoiti in Belgium. Pathogens (Basel, Switzerland). 2021;10(12).
20. Liénard E. Development of a protocol testing the ability of Stomoxys calcitrans (Linnaeus, 1758) (Diptera: Muscidae) to transmit Besnoitia besnoiti (Henry, 1913) (Apicomplexa: Sarcocystidae). Parasitology research. 2013;112(2):479–86.
21. Bigalke RD. New Concepts on the Epidemiological Features of Bovine Besnoitiosis as Determined by Laboratory and Field Investigations. The Onderstepoort journal of veterinary research. 1968;35(1):3–137.
22. Parsonson IM. Pathology and pathogenesis of bluetongue infections. Current topics in microbiology and immunology. 1990;162:119–41.
23. Barcélo CM, M.A. Bionomics of livestock-associated Culicoides (biting midge) bluetongue virus vectors under laboratory conditions. Medical and Veterinary Entomology. 2018;32(2).
24. Alvarez-García G. A century of bovine besnoitiosis: an unknown disease re-emerging in Europe. Trends in parasitology. 2013;29(8):407–15.
25. Gazzonis AL. Serological dynamics and risk factors of Besnoitia besnoiti infection in breeding bulls from an endemically infected purebred beef herd. Parasitology research. 2017;116(4):1383–93.
26. Hornok S. Screening of bat faeces for arthropod-borne apicomplexan protozoa: Babesia canis and Besnoitia besnoiti-like sequences from Chiroptera. Parasites & vectors. 2015;8:450.
27. Esteban-Gil A. No detection of Besnoitia besnoiti DNA in the semen of chronically infected bulls. Parasitology research. 2014;113(6):2355–62.
28. Frey CF. Chronic bovine besnoitiosis: intra-organ parasite distribution, parasite loads and parasite-associated lesions in subclinical casesx. Veterinary Parasitology. 2013;197(1-2):95–103.
29. Alvarez-García G. Seroprevalence of Besnoitia besnoiti infection and associated risk factors in cattle from an endemic region in Europe. Veterinary journal (London, England : 1997). 2014;200(2):328–31.
30. Esteban-Gil A. Epidemiological patterns of bovine besnoitiosis in an endemic beef cattle herd reared under extensive conditions. Veterinary parasitology. 2017;236:14–21.
31. Schulz KCA. A report on naturally acquired Besnoitiosis in bovines with special reference to its pathology. Journal of the South African Veterinary Association. 1960;31(1):21–36.
32. Bigalke RD. Besnoitiosis and Globidiosis. In: Ristic M, McIntyre I, editors. Diseases of Cattle in the Tropics: Economic and Zoonotic Relevance. Dordrecht: Springer Netherlands; 1981. p. 429–42.
33. Cortes H. A review on bovine besnoitiosis: a disease with economic impact in herd health management, caused by Besnoitia besnoiti (Franco and Borges, ). Parasitology. 2014;141(11):1406–17.
34. Ramakrishnan C. Dissection of Besnoitia besnoiti intermediate host life cycle stages: From morphology to gene expression. PLoS pathogens. 2022;18(11):e1010955.
35. Basson PA. Observations on the pathogenesis of bovine and antelope strains of Besnoitia besnoiti (Marotel, 1912) infection in cattle and rabbits. The Onderstepoort journal of veterinary research. 1970;37(2):105–26.
36. Gollnick NS. Natural Besnoitia besnoiti infections in cattle: chronology of disease progression. BMC veterinary research. 2015;11:35.
37. Langenmayer MC. Naturally acquired bovine besnoitiosis: histological and immunohistochemical findings in acute, subacute, and chronic disease. Veterinary pathology. 2015;52(3):476–88.
38. Gollnick NS. Naturally acquired bovine besnoitiosis: Disease frequency, risk and outcome in an endemically infected beef herd. Transboundary and emerging diseases. 2018;65(3):833–43.
39. Gutiérrez-Expósito D. Advances in the diagnosis of bovine besnoitiosis: current options and applications for control. International journal for parasitology. 2017;47(12):737–51.
40. Espinosa G. Bovine PMN responses to extracellular vesicles released by Besnoitia besnoiti tachyzoites and B. besnoiti-infected host cells. Frontiers in immunology. 2024;15:1509355.
41. Turra N. Besnoitia besnoiti-Induced Neutrophil Extracellular Traps (NETs): Metabolic Signature, Signaling Pathways, Receptors and Implications on Pathogenesis. Animals : an open access journal from MDPI. 2025;15(22).
42. Neuman M. Serological survey of Besnoitia besnoiti (Marotel 1912) infection in Israel by immunofluorescence. Zentralblatt fur Veterinarmedizin Reihe B Journal of veterinary medicine Series B. 1972;19(5):391–6.
43. Bigalke RD. The relationship between Besnoitia of antelopes and besnoitia besnoiti (Marotel, 1912) of cattle. Bulletin – Office international des epizooties. 1966;66(1):903–5.
44. Oryan A, Ahmadi A, Kamali A, Hajjafari A. Global Impact of Emerging Besnoitiosis on Cattle: Effects on Production, Fertility, and Economic Losses with an Update on Worldwide Besnoitia Infection. The Microbe. 2025:100590.
45. Villa L. Bovine besnoitiosis in an endemically infected dairy cattle herd in Italy: serological and clinical observations, risk factors, and effects on reproductive and productive performances. Parasitology research. 2019;118(12):3459–68.
46. Anastácio C. Impact of Endemic Besnoitiosis on the Performance of a Dairy Cattle Herd. Animals : an open access journal from MDPI. 2022;12(10).
47. Pouchard L. Santé animale : Gare à la besnoitiose bovine La France Agricole2022 [updated 03–07–2025. Available from: https://www.lafranceagricole.fr/sommet-de-l-elevage/article/776178/gare-a-la-besnoitiose-bovine.
48. Cortes HCE. Application of conventional and real-time fluorescent ITS1 rDNA PCR for detection of Besnoitia besnoiti infections in bovine skin biopsies. Veterinary parasitology. 2007;146(3-4):352–6.
49. Jacinto J. Bovine besnoitiosis: Assessment of the diagnostic accuracy of three different tests using a Bayesian latent class model approach and clinical characterization of the disease. Preventive veterinary medicine. 2025;235:106415.
50. Cortes HCE. Immunodiagnosis of Besnoitia besnoiti infection by ELISA and Western blot. Veterinary parasitology. 2006;141(3-4):216–25.
51. Cortes HCE. In vitro effects of arylimidamides against Besnoitia besnoiti infection in Vero cells. Parasitology. 2011;138(5):583–92.
52. Jiménez-Meléndez A. In vitro efficacy of bumped kinase inhibitors against Besnoitia besnoiti tachyzoites. International journal for parasitology. 2017;47(12):811–21.
53. Shkap V. Besnoitia besnoiti: chemotherapeutic trials in vivo and in vitro. Revue d’elevage et de medecine veterinaire des pays tropicaux. 1987;40(3):259–64.
54. Müller J. In vitro treatment of Besnoitia besnoiti with the naphto-quinone buparvaquone results in marked inhibition of tachyzoite proliferation, mitochondrial alterations and rapid adaptation of tachyzoites to increased drug concentrations. Parasitology. 2019;146(1):112–20.
55. Jiménez-Meléndez A. Repurposing of commercially available anti-coccidials identifies diclazuril and decoquinate as potential therapeutic candidates against Besnoitia besnoiti infection. Veterinary parasitology. 2018;261:77–85.
56. Eberhard N. Activities of Endochin-Like Quinolones Against in vitro Cultured Besnoitia besnoiti Tachyzoites. Frontiers in veterinary science. 2020;7:96.
57. Olias P. Molecular pathology, taxonomy and epidemiology of Besnoitia species (Protozoa: Sarcocystidae). Infection, genetics and evolution : journal of molecular epidemiology and evolutionary genetics in infectious diseases. 2011;11(7):1564–76.
58. GD. Voorkom insleep van dierziekten via aanvoer van runderen.

