TEKST ROBERT-JAN MOLENAAR, PLUIMVEE DIERENARTS EN PATHOLOOG, ROYAL GD
Pluimveepathologie
Voor de diergezondheidsmonitoring doet Royal GD jaarlijks circa twaalfhonderd secties op pluimvee. Elke inzending van pluimvee voor pathologisch onderzoek bestaat normaal gesproken uit meerdere dieren, waarbij het belangrijk is dat de inzender dieren selecteert die representatief zijn voor het gezondheidsprobleem dat onderzocht moet worden. Dit is een groot verschil met het pathologisch onderzoek zoals we dat kennen bij bijvoorbeeld rundvee of gezelschapsdieren, waar vaak een enkel dier onderzocht wordt en waarbij de zoektocht gericht is op het vinden van de doodsoorzaak en eventueel onderliggend lijden.

Foto 1. Pathologisch onderzoek op ingezonden vleeskuikens in de sectiezaal van GD.
Bij koppelgehouden dieren zoals kippen wordt onderzoek gedaan naar een koppelprobleem. Dat hoeft niet primair sterfte te zijn, maar het kan bijvoorbeeld ook gaan om diarree, eiproductiedaling of verminderde voeropname. In zo’n geval vindt het onderzoek plaats bij klinische representanten en dat kan betekenen dat er voor een gedegen onderzoek levende dieren moeten worden aangeboden.
LEVENDE DIEREN
Levende dieren zijn nodig om klinisch onderzoek te kunnen doen voorafgaand aan de sectie, zoals bij locomotiestoornissen. Op basis van de anamnese en de klinische bevindingen wordt gericht vervolgonderzoek gekozen bij de sectie, bijvoorbeeld bij aanwijzingen voor een neurologische oorsprong van de bewegingsproblemen, op de hersenen van de sterkst aangetaste dieren. Maar het kan ook nodig zijn levende dieren aan te leveren, omdat sommige vervolgonderzoeken uitgevoerd moeten worden op weefsels die je zeer kort na de dood moet verzamelen. Denk hierbij aan microscopisch onderzoek op de darmen en de kweek van sommige bacteriële pathogenen zoals Avibacterium paragallinarum of Mycoplasma spp. Omdat de dieren (nog) niet zijn doodgegaan aan de ziekte die onderzocht moet worden, of omdat er gekeken wordt naar ziekten die helemaal niet tot ernstige letsels leiden, zijn de macroscopische bevindingen bij dergelijke secties vaak minder uitgesproken. De pluimveepatholoog is in zulke gevallen in grotere mate afhankelijk van vervolgonderzoek en van de kwaliteit van de aangeleverde anamnese. Natuurlijk komt het ook veel voor dat de inzender wil weten wat de oorzaak van verhoogde uitval is en dan dienen er juist wel dode dieren ingestuurd te worden en lijkt het proces al een stuk meer op de ‘normale’ pathologie zoals we die bij andere diersoorten kennen.
VERVOLGONDERZOEKEN
Het onderzoek naar koppelproblemen is in zekere zin een ‘second opinion’, want de inzendende practicus heeft hetzelfde probleem al onderzocht en zal hierbij vaak ook al op enkele dieren sectie hebben uitgevoerd. De toegevoegde waarde van het pathologisch onderzoek bij GD zit hem dan ook niet enkel in een vers paar ogen dat naar het probleem kijkt, maar juist in de vervolgonderzoeken die GD kan inzetten. De brede reikwijdte aan onderzoeken die GD beschikbaar heeft, komt hierbij deels voort uit de secties. Wanneer tijdens de sectie een nieuwe (variatie van een) pathogeen wordt gevonden, kan worden gekeken of de huidige diagnostiek nog afdoende is, of dat er aanpassingen moeten worden gedaan. Omdat de hele werkwijze aanzienlijk verschilt ten opzichte van secties op zoogdieren, voert GD de pluimveepathologie uit in een aparte sectiezaal en door andere pathologen. In de regel besteden deze pathologen een deel van hun tijd aan andere activiteiten, zoals wetenschappelijk onderzoek naar pluimveeziekten, en zijn ze ingebed in het pluimveeteam van GD.
VLEESKUIKENS MET LOCOMOTIESTOORNIS
Ter illustratie bespreken we kort een sectie op vleeskuikens met locomotiestoornis door virale tenosynovitis, een ziekte die de afgelopen jaren voor veel problemen heeft gezorgd. Bij het klinisch onderzoek op de ingezonden dieren viel op dat ze te stijl op de poten stonden, dat de hakpees verdikt was en dat de dieren stram liepen, maar de reflexen waren wel in orde. Tijdens de sectie werden geen afwijkingen gezien aan de gewrichten of groeischijven en de peesschede was ter hoogte van de metatarsus verdikt met een zeer vochtig aspect bij aansnede. Het beeld paste sterk bij virale tenosynovitis, een diagnose die de inzendend dierenarts op basis van het stalbeeld ook al had gesteld. Deze ziekte wordt veroorzaakt door een reovirus. Reovirussen komen relatief vaak voor in de darmen van gezonde vleeskuikens en de meeste stammen zijn niet in staat om tenosynovitis te veroorzaken. Enkel PCR-onderzoek uitvoeren op aanwezigheid van reovirus blijkt dan ook onvoldoende om de diagnose te stellen. Maar alleen macroscopisch onderzoek is ook onbetrouwbaar vanwege de kans op zowel vals-positieve als vals-negatieve bevindingen. Bij de sectie wordt daarom naast het macroscopisch onderzoek en de PCR-test ook histologisch onderzoek uitgevoerd op de pees en peesschede. Op basis hiervan kan worden gekeken of er sprake is van een beeld passend bij virale tenosynovitis (foto 2); dit is belangrijk om onderscheid te kunnen maken met differentiële diagnoses zoals infectie met Mycoplasma synoviae of stafylokokken.
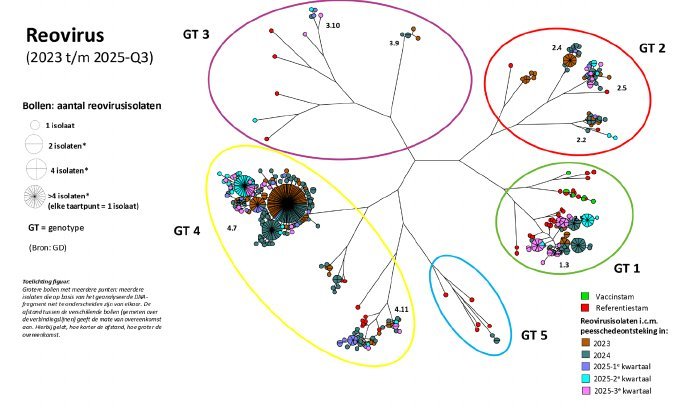
Figuur 1. Resultaten van genotypering van reovirusstammen uitgevoerd door GD (2023 t/m 3e kwartaal 2025) (Bron: GD-monitoringsdata).
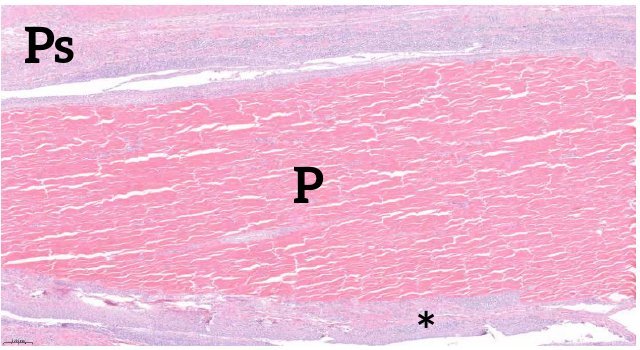
Foto 2. Histologisch beeld van een pees (P) met peesschede (Ps) van een vleeskuiken met virale tenosynovitis. De pees is omringd door een laag ontstekingscellen (peritendinitis) (*) en de omringende vliezen zijn sterk verdikt door eenzelfde lymfoplasmacellulair ontstekingsinfiltraat.
De combinatie van PCR en histologie is voldoende voor een diagnose. Bovendien wordt op het PCR-product een nadere genotypering uitgevoerd. Aan de hand hiervan kan inzicht verkregen worden in de epidemiologie (figuur 1). Als er bij nakomelingen van eenzelfde koppel vermeerderingspluimvee clusters met een identiek reovirus worden aangetoond, kan men bijvoorbeeld denken aan verticale overdracht van het virus. Anderzijds kan een terugkerende infectie in eenzelfde stal met hetzelfde virus wijzen op onvoldoende reiniging en desinfectie tijdens de periode van leegstand tussen twee koppels.
Wat opvalt in figuur 1, is dat een groot aantal isolaten dicht bij elkaar ligt, dit cluster noemen we genotype (GT) 4.7. Dit genotype is sterk in opkomst sinds het begin van de huidige golf aan reovirusproblemen. In eerste instantie is de spreiding van dit specifieke reovirus in kaart gebracht. Door deze monitoringsbevinding was het voor GD vervolgens mogelijk een voorstel te doen voor passend wetenschappelijk onderzoek. In opdracht van AVINED voert GD daarom nu onderzoek uit naar de virulentie van GT4.7, maar ook naar de mogelijkheid neutraliserende antistoffen tegen GT4.7 op te wekken met bestaande vaccins en onderzoek naar een serologische test om de werking van eventuele autovaccins te kunnen onderbouwen.
CONCLUSIE
Wat begint als pathologisch onderzoek naar een ziekte die de practicus in de basis ook zelf kan diagnosticeren, leidt dus tot een stevigere diagnose op basis van de combinatie van histologie en PCR, tot een onderbouwing van eventuele verticale spreiding, tot opheldering van mogelijk verwante uitbraken en uiteindelijk ook tot verbeterde diagnostiek en inzicht in de mogelijkheden van vaccinaties.

